「禁忌を含む使用上の注意」等は電子添文をご参照ください
臨床成績 国内第Ⅲ相長期投与試験
(維持血液透析下の二次性副甲状腺機能亢進症患者を対象とした長期投与試験)[AJ1003試験]
社内資料:第Ⅲ相試験-長期投与試験
-維持血液透析下の二次性副甲状腺機能亢進症患者を対象とした長期投与試験-(承認時評価資料)
試験概要
- 目的
-
維持血液透析下の二次性副甲状腺機能亢進症(SHPT)患者を対象に、ウパシタを52週間投与したときの安全性及び有効性について検討する。
- 対象
-
維持血液透析下のSHPT患者 157例
[主な選択基準]週3回の血液透析又は血液透析ろ過を施行する安定期の慢性腎不全患者、最大透析間隔後の透析前血清iPTH濃度が240pg/mLを超え、かつ最大透析間隔後の透析前血清補正Ca濃度が8.4mg/dL以上の患者
- 試験デザイン
-
多施設共同、非盲検、非対照
- 方法
-
ウパシタを週3回、血液透析終了時の返血時に透析回路静脈側に用量調整して投与した。期間は52週間とした。なお、前治療薬(CaSR作動薬)がある場合はWash out期間を設けた。
[開始用量]試験薬投与開始1週間前の血清補正Ca濃度が9.0mg/dL未満の場合は25μg、9.0mg/dL以上の場合は50μgとした。
[用量調整方法]患者の血清iPTH濃度を60~240pg/mLの範囲に維持することを目標に、用量を25~300μgの範囲で調整した。なお、用量調整は25、50、100、150、200、250及び300μgの7段階で行うこととした。
[臨床検査]iPTH、Ca、Pは、スクリーニング時、0~24週は毎週、24~52週は2週毎又は中止時の透析前に採血した。副甲状腺エコーは、スクリーニング時、24、52週又は中止時に実施した。
- 評価項目
-
有効性評価項目
・各時点における血清iPTH濃度の目標達成率※1
・各時点における下記項目の測定値
血清iPTH濃度、血清補正Ca濃度、血清P濃度・各時点における副甲状腺体積 等
安全性評価項目
有害事象及び副作用、臨床検査値 等
- 解析計画
-
有効性評価項目
有効性評価のための主要解析対象集団は最大の解析対象集団であるFAS(Full Analysis Set)とした。
・各時点における血清iPTH濃度が60pg/mL以上240pg/mL以下を達成した患者割合及び両側95%信頼区間を算出した。なお、データが欠測の時点は、割合を算出する際の母数に含めずに計算した。
・各時点における下記項目の測定値について要約統計量を算出し、患者、時点を因子とした繰り返しのない二元配置分散分析を行った。
血清iPTH濃度、血清補正Ca濃度、血清P濃度・各時点における副甲状腺体積及び副甲状腺の長径の要約統計量を算出し、患者、時点を因子とした繰り返しのない二元配置分散分析を用いて因子の影響について検討した。
安全性評価項目
副作用について各事象の発現例数及び発現率を算出した。また、注目すべき事象として上部消化管障害、下部消化管障害、低カルシウム血症及び血清補正Ca濃度の低下について、発現例数及び発現率を算出した。
投与状況
試験薬投与量別の患者割合を算出した。
※1:血清iPTH濃度が60pg/mL以上240pg/mL以下を達成した患者の割合
7. 用法及び用量に関連する注意(抜粋)
7.4 増量する場合には増量幅を50μg(ただし25μgから増量する場合は50μgへ増量)とし、2週間以上の間隔をあけて行うこと。
試験デザイン
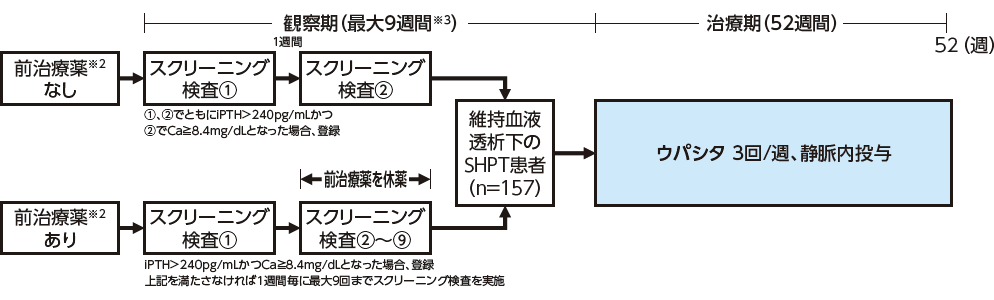
- ※2:シナカルセト又はエテルカルセチド
- ※3:観察期は前治療薬なしの場合は2週間、前治療薬ありの場合は最大9週間とした
有効性
[血清iPTH]
投与後52 週の血清iPTH濃度の目標達成率※は、94.2%[95%信頼区間:89.0%-97.5%]であった。
※:血清iPTH濃度が60pg/mL以上240pg/mL以下を達成した患者の割合
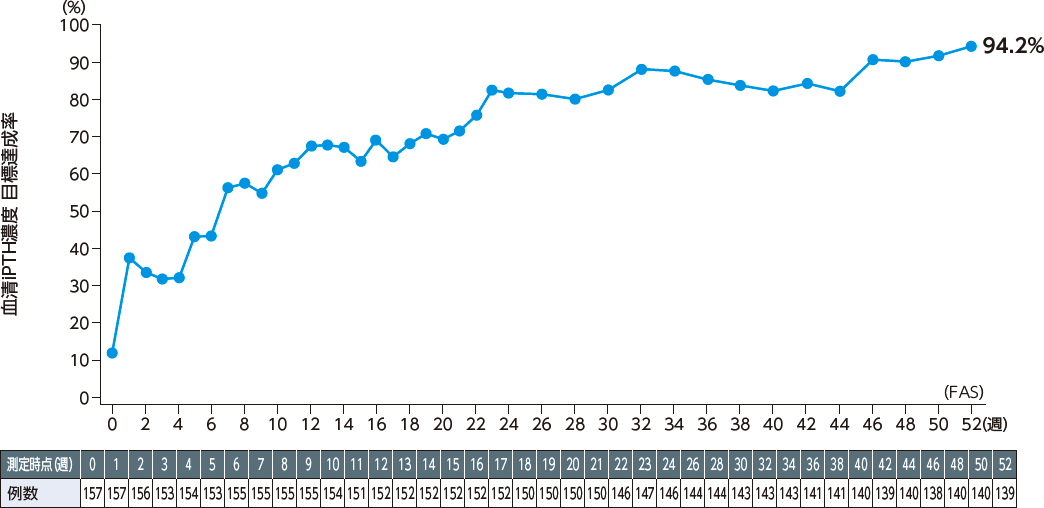
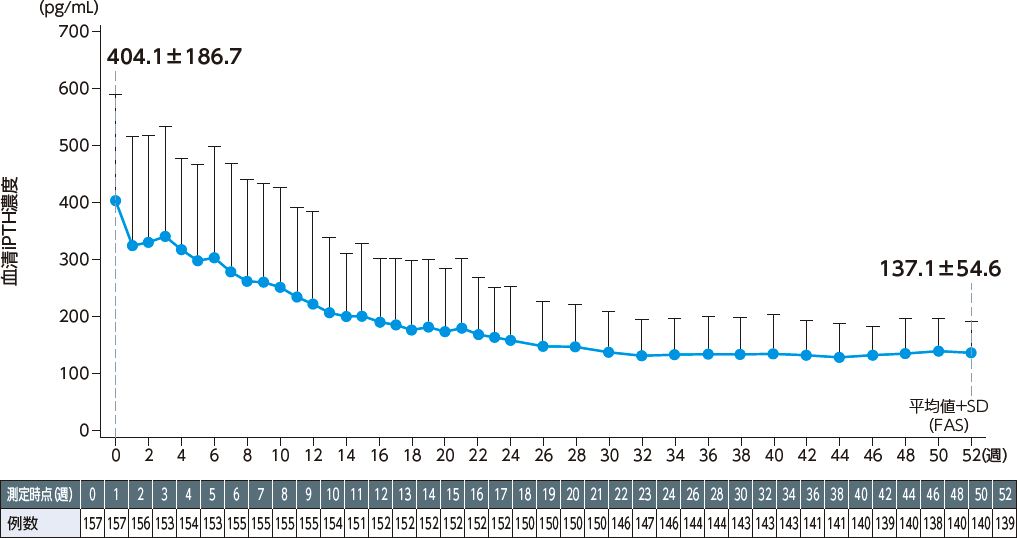
投与52週までの血清iPTH濃度の推移について、統計学的な有意差が認められた。
(p<0.001、二元配置分散分析)
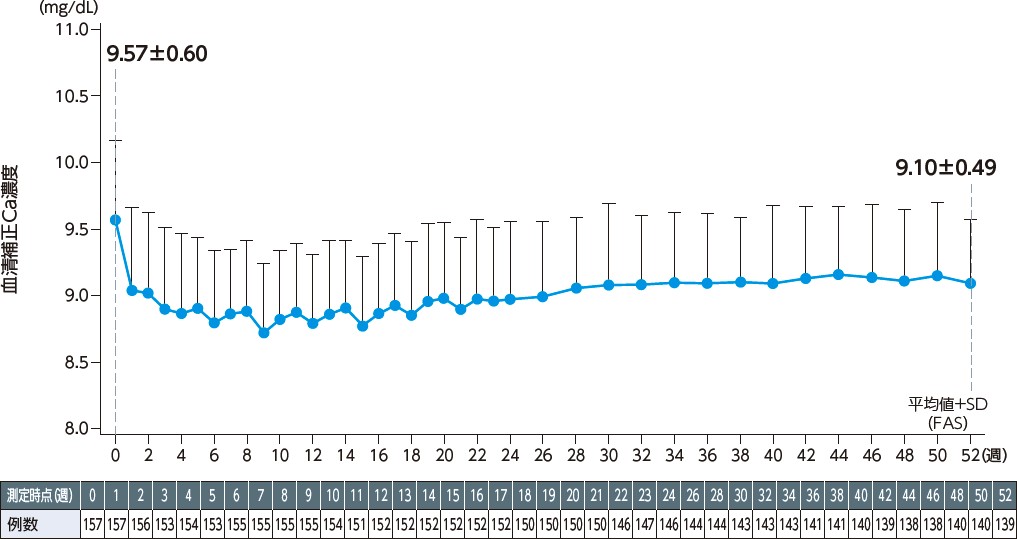
[血清補正Ca]
投与52週までの血清補正Ca濃度の推移について、統計学的な有意差が認められた。
(p<0.001、二元配置分散分析)
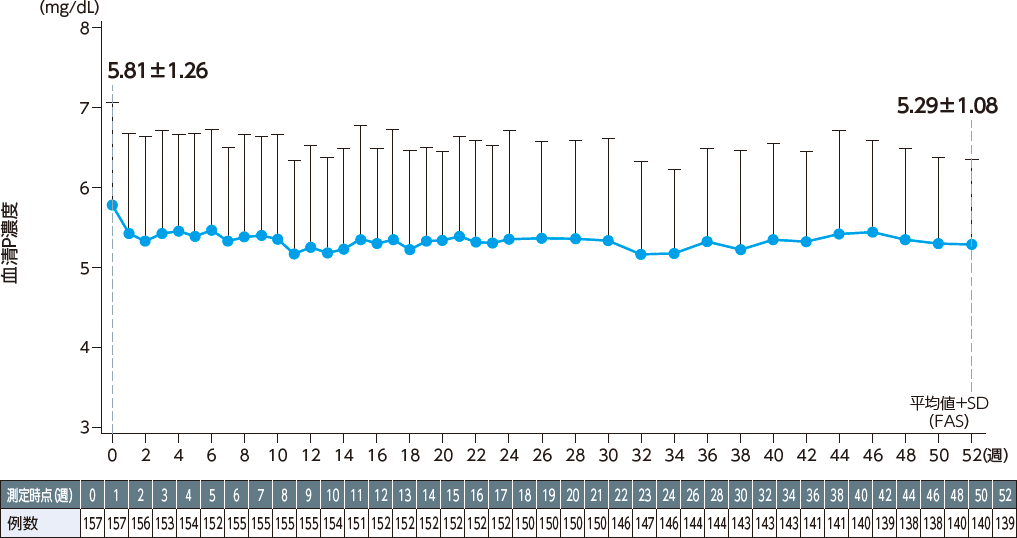
[血清P]
投与52週までの血清P濃度の推移について、統計学的な有意差が認められた。
(p=0.0171、二元配置分散分析)
[副甲状腺体積]
投与52週までの副甲状腺体積の推移について、統計学的な有意差が認められた。
(p=0.0065、二元配置分散分析)
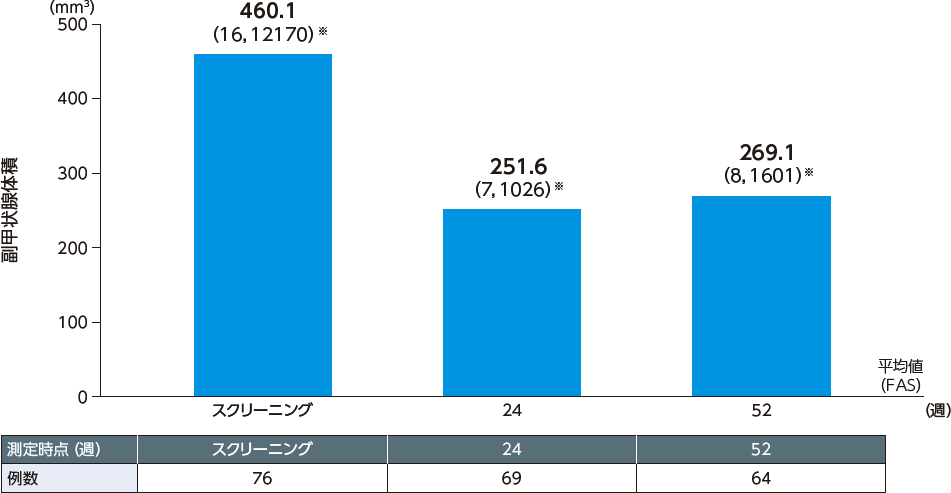
※:平均値(範囲)
投与量別の患者割合の推移
投与量別の患者割合の推移は以下の通りであった。最終投与量は25μg が19.7%、50μg が22.9%、100μg が16.6%、150μgが10.8%であり、7割が25~150μgであった。
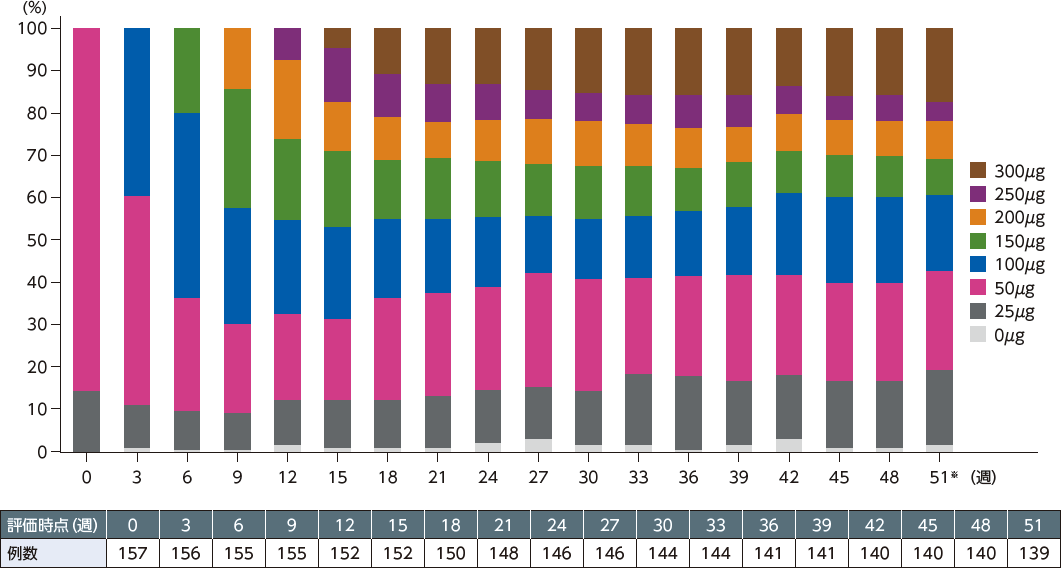
※:51週については3回目投与量、その他の週については1回目投与量を示す
安全性
157例中10例(6.4%)に副作用が認められた。
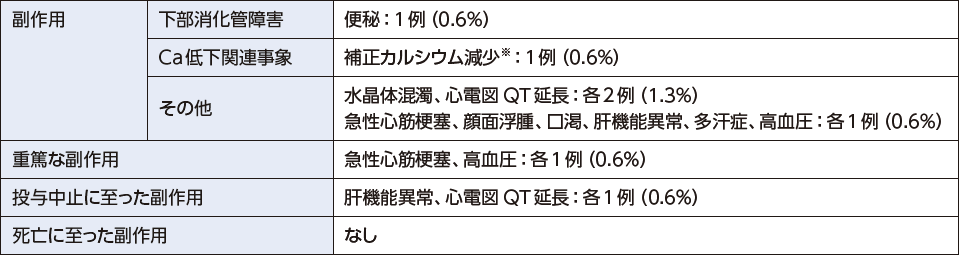
- 集計にはMedDRA/J(バージョン21.1)のPT及びSOCを用いた。
- ※:無症候性のカルシウム減少を「補正カルシウム減少」として集計
